THYROID-LIT. 50969
Apatinib vs Placebo in patients with locally advanced or metastatic, radioactive iodine-refractory differentiated thyroid cancer – the REALITY randomized clinical trial.
Lin, Y.; Qin, S.; Li, Z.; Yang, H.; Fu, W.; Li, S.; Chen, W.; Gao, Z.; Miao, W.; Xu, H.; Zhang, Q.; Zhao, X.; Bao, J.; Li, L.; Ren, Y.; Lin, C.; Jing, S.; Ma, Q.; Liang, J.; Chen, G.; Zhang, H.; Zhang, Y.; Zhou, X.; Sang, Y.; Hou, Z.
(Dept. of Nuclear Medicine, Beijing Key Laboratory of Molecular Targeted Diagnosis and Therapy in Nuclear Medicine, State Key Laboratory of Complex Severe and Rare Diseases, Peking Union Medical College Hospital, Chinese Academy of Medical Science and Peking Union Medical College, Beijing; Dept. of Oncology, Cancer Center of Bayi Hospital, Nanjing Chinese Medicine University, Nanjing, all China)
JAMA Oncology 8: 242-250 (2022)
Die Prognose bei Patienten mit einem radiojodrefraktären differenzierten Schilddrüsenkarzinom ist schlecht.
In den letzten Jahren wurden Substanzen wie Sorafenib oder Lenvatinib untersucht, die eine Hemmung der Angiogenese herbeiführen. Auch die hier untersuchte Substanz, Apatinib, ist ein Hemmstoff der Angiogenese, die sehr selektiv den „vascular endothelial growth factor“ (VEGFR-2) hemmt.
Berichtet wird in dieser prospektiven, placebokontrollierten Doppelblindstudie über 92 Patienten (56 Frauen, 36 Männer) mit einem progredienten lokal fortgeschrittenen oder metastasierten differenzierten Schilddrüsenkarzinom. Das Alter betrug 55,7 ± 10,6 Jahre. Verabreicht wurden 500 mg Apatinib/Tag p. o. oder ein Placebo. Primärer Endpunkt war das progressionsfreie Überleben PFS. Sekundäre Endpunkte waren das Gesamtüberleben, die Responserate, die Dauer der Response und weitere Parameter. Es erfolgte eine Interimsanalyse.
Die Nachbeobachtungszeit belief sich auf 18,1 Monate (Median; Interquartilbereich IQR 12,7–22,2 Monate). Das PFS lag im Median bei 22,2 Monaten (IQR 10,91– nicht erreicht) in der Apatinibgruppe und 4,5 Monaten (IQR 1,94–9,17) in der Placebogruppe (vgl. Abb. Teil A). Die Hazard Ratio betrug 0,26, der 95 %-Vertrauensbereich CI 0,14–0,47 (p < 0,001). Das PFS nach 12 Monaten errechnete sich mit 60,3 % (95 % CI 40,8–75,2 %) in der Apatinibgruppe und 12,4 % (95 % CI 3,4–27,4 %) in der Placebogruppe. Nach 24 Monaten betrug das PFS 37,2 % in der Apatinibgruppe (95 % CI 15,1–59,7 %) und 4,1 % in der Placebogruppe (95 % CI 0,3–17,2 %). Die Gesamtüberlebensrate (overall survival OS; Median) wurde in der Apatinibgruppe nicht erreicht und betrug 29,9 Monate (95 % CI 18,96– nicht erreicht) in der Placebogruppe. Dies zeigt Teil B der Abbildung.
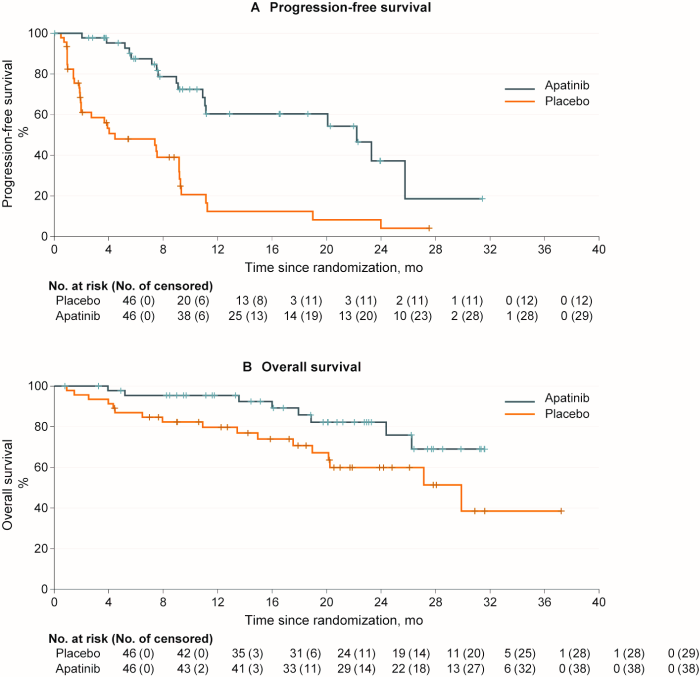
Auch weitere sekundäre Endpunkte wie die gesamte Responserate (overall response rate) zeigten eine Überlegenheit der Apatinibeinnahme. Die unerwünschten Wirkungen von Apatinib beinhalten das Hand-Fuß-Syndrom. Daneben wurden Proteinurie, Diarrhö oder ein Blutdruckanstieg verzeichnet.
In dieser randomisierten und placebokontrollierten Studie zeigte somit Apatinib einen signifikanten Vorteil. Sowohl das PFS als auch das Gesamtüberleben (OS) fiel deutlich günstiger aus, wenn Apatinib verabreicht wurde.
Letzte Aktualisierung: 20.07.2022










.jpg 767w, /dam/jcr:81e7bab5-e57d-4702-94bd-ecf4c7aadc8f/10_4235_0033_Joppen_500%20(1).jpg 1200w)











